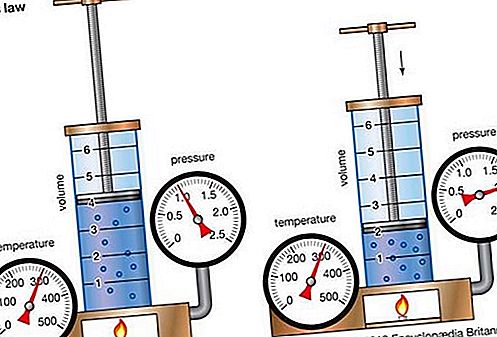
Undang-undang Boyle, juga disebut hukum Mariotte, hubungan mengenai pemampatan dan pengembangan gas pada suhu tetap. Hubungan empirik ini, yang dirumuskan oleh ahli fizik Robert Boyle pada tahun 1662, menyatakan bahawa tekanan (p) kuantiti gas yang diberikan berbeza-beza dengan isipadu (v) pada suhu tetap; iaitu, dalam bentuk persamaan, pv = k, pemalar. Hubungan itu juga ditemui oleh ahli fizik Perancis Edme Mariotte (1676).
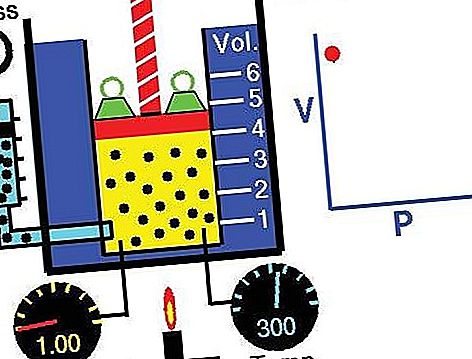
Undang-undang tersebut dapat diturunkan dari teori kinetik gas dengan menganggap gas sempurna (ideal) (lihat gas sempurna). Gas nyata mematuhi undang-undang Boyle pada tekanan yang cukup rendah, walaupun produk pv pada umumnya menurun sedikit pada tekanan yang lebih tinggi, di mana gas mula berlepas dari tingkah laku ideal.