Ciri-ciri fizikal
Air mempunyai beberapa sifat fizikal yang penting. Walaupun sifat-sifat ini tidak asing lagi kerana adanya air di mana-mana, sebahagian besar sifat fizikal air agak tidak biasa. Memandangkan jisim molar molekul penyusunnya yang rendah, air mempunyai nilai kelikatan yang luar biasa besar, tegangan permukaan, haba pengewapan, dan entropi pengewapan, yang semuanya dapat dikaitkan dengan interaksi ikatan hidrogen yang luas yang terdapat dalam air cair. Struktur ais terbuka yang memungkinkan ikatan hidrogen maksimum menjelaskan mengapa air pepejal kurang padat daripada air cair - keadaan yang sangat luar biasa di antara bahan biasa.
| Ciri fizikal air terpilih | |
|---|---|
| jisim molar | 18.0151 gram setiap mol |
| takat lebur | 0.00 ° C |
| takat didih | 100.00 ° C |
| ketumpatan maksimum (pada 3.98 ° C) | 1.0000 gram setiap sentimeter padu |
| ketumpatan (25 ° C) | 0,99701 gram per sentimeter padu |
| tekanan wap (25 ° C) | 23.75 torr |
| haba pelakuran (0 ° C) | 6.010 kilojoule per mol |
| haba pengewapan (100 ° C) | 40.65 kilojoule per mol |
| haba pembentukan (25 ° C) | −285.85 kilojoule per mol |
| entropi pengewapan (25 ° C) | 118.8 joule per ° C mol |
| kelikatan | 0.8903 centipoise |
| ketegangan permukaan (25 ° C) | 71.97 dynes per sentimeter |
Sifat kimia
Tindak balas asid-asas
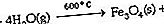
Air mengalami pelbagai jenis tindak balas kimia. Salah satu sifat kimia penting air adalah keupayaannya untuk bertindak sebagai asid (penderma proton) dan basa (akseptor proton), sifat ciri zat amfoterik. Tingkah laku ini paling jelas dilihat pada pengionan air: H 2 O (l) + H 2 O (l) ⇌ H 3 O + (aq) + OH - (aq), di mana (l) mewakili keadaan cecair, (aq) menunjukkan bahawa spesies tersebut dilarutkan di dalam air, dan anak panah berganda menunjukkan bahawa tindak balas boleh berlaku di kedua-dua arah dan keadaan keseimbangan wujud. Pada suhu 25 ° C (77 ° F) kepekatan H + terhidrat (iaitu, H 3 O +, yang dikenali sebagai ion hidronium) di dalam air ialah 1.0 × 10 −7 M, di mana M mewakili mol per liter. Kerana satu OH - ion dihasilkan untuk setiap H 3 O + ion, kepekatan OH - pada 25 ° C juga 1,0 × 10 -7 M. air Dalam pada 25 ° C H 3 O + kepekatan dan OH - kepekatan mestilah sentiasa 1.0 × 10 −14: [H +] [OH -] = 1.0 × 10 −14, di mana [H +] mewakili kepekatan ion H + terhidrat dalam mol per liter dan [OH -] mewakili kepekatan OH - ion dalam mol per liter.
Apabila asid (bahan yang dapat menghasilkan ion H +) larut dalam air, asid dan air menyumbang ion H + ke dalam larutan. Ini membawa kepada keadaan di mana kepekatan H + lebih besar daripada 1.0 × 10 −7 M. Oleh kerana mesti selalu benar bahawa [H +] [OH -] = 1.0 × 10 −14 pada 25 ° C, [OH -] mesti diturunkan ke beberapa nilai di bawah 1.0 × 10 −7. Mekanisme untuk mengurangkan kepekatan OH - melibatkan tindak balas H + + OH - → H 2 O, yang berlaku setakat yang diperlukan untuk memulihkan produk [H +] dan [OH -] hingga 1.0 × 10 −14 M. Oleh itu, apabila asid ditambahkan ke dalam air, larutan yang dihasilkan mengandungi lebih banyak H + daripada OH -; iaitu, [H +]> [OH -]. Penyelesaian seperti itu (di mana [H +]> [OH -]) dikatakan berasid.
Kaedah yang paling umum untuk menentukan keasidan larutan adalah pHnya, yang ditakrifkan dari segi kepekatan ion hidrogen: pH = −log [H +], di mana log simbol bermaksud logaritma asas-10. Dalam air tulen, di mana [H +] = 1.0 × 10 −7 M, pH = 7.0. Untuk larutan berasid, pH kurang dari 7. Apabila asas (bahan yang bertindak sebagai akseptor proton) dilarutkan dalam air, kepekatan H + menurun sehingga [OH -]> [H +]. Penyelesaian asas dicirikan dengan mempunyai pH> 7. Ringkasnya, dalam larutan berair pada 25 ° C:
| penyelesaian neutral | [H +] = [OH -] | pH = 7 |
| larutan berasid | [H +]> [OH -] | pH <7 |
| penyelesaian asas | [OH -]> [H +] | pH> 7 |