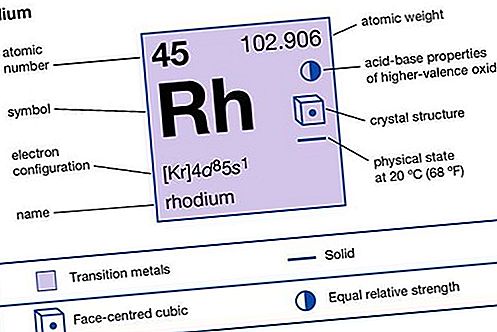
Rhodium (Rh), unsur kimia, salah satu logam platinum dari Kumpulan 8-10 (VIIIb), Periode 5 dan 6, dari jadual berkala, terutama digunakan sebagai agen paduan untuk mengeras platinum. Rhodium adalah logam putih perak yang berharga, dengan daya kilauan tinggi untuk cahaya. Ia tidak berkarat atau tercemar oleh suasana pada suhu bilik dan sering disadur ke objek logam dan digilap untuk memberikan permukaan tetap dan menarik untuk perhiasan dan barang hiasan lain. Logam ini juga digunakan untuk menghasilkan permukaan pantulan untuk instrumen optik.
Rhodium yang ditambahkan ke platinum dalam jumlah kecil menghasilkan aloi yang lebih keras dan menurunkan berat badan pada suhu tinggi bahkan lebih perlahan daripada platinum tulen. Aloi seperti itu digunakan untuk kerucut tungku makmal, elektrod palam pencucuh, dan pemangkin di persekitaran kimia yang sangat panas (termasuk penukar pemangkin kenderaan). Dalam pembuatan asid nitrik industri, pemangkin kasa dari aloi rhodium – platinum digunakan kerana ia dapat menahan suhu nyala api kerana amonia dibakar menjadi oksida nitrat. Kawat aloi 10% rhodium – 90 peratus platinum yang bergabung dengan dawai platinum tulen membentuk termokopel yang sangat baik untuk mengukur suhu tinggi dalam suasana pengoksidaan. Skala suhu antarabangsa ditentukan di rantau ini dari 660 ° hingga 1,063 ° C (1,220 ° hingga 1,945 ° F) oleh daya elektromotif termokopel ini.
Rhodium adalah unsur langka yang terdiri daripada 4.6 peratus aloi platinum asli. Ia juga berlaku pada aloi asli iridium dan osmium: sekurang-kurangnya 11.25 peratus dalam iridosmine dan sekurang-kurangnya 4.5 peratus pada siserskite. Rhodium berlaku secara semula jadi dalam hubungannya dengan logam platinum yang lain, dan pemisahan dan penyempurnaannya menjadi sebahagian daripada pemprosesan metalurgi keseluruhan kumpulan. Rhodium umumnya diperoleh secara komersial sebagai hasil sampingan dari pengekstrakan nikel dan tembaga dari bijihnya.
Rhodium semula jadi terdiri sepenuhnya dari isotop stabil rhodium-103. Unsur ini pertama kali diasingkan (1803) dari platinum mentah oleh ahli kimia dan ahli fizik Inggeris William Hyde Wollaston, yang menamakannya dari rhodon Yunani ("mawar") untuk warna merah sejumlah sebatiannya. Rhodium sangat tahan terhadap serangan asid; logam besar tidak dilarutkan oleh asid nitrik atau hidroklorik pekat panas atau bahkan oleh aqua regia. Logam larut dalam kalium hidrogen sulfat menyatu untuk menghasilkan sulfat larut dalam air K 3 Rh (SO 4) 3 · 12H 2 O, dalam asid sulfurik pekat panas, dan dalam asid hidroklorik pekat yang mengandung natrium perklorat pada 125 ° -150 ° C (257 ° –302 ° F).
Kimia rhodium berpusat terutamanya pada keadaan pengoksidaan +1 dan +3; beberapa sebatian dari keadaan pengoksidaan positif yang lain melalui +6 dikenali. Rhodium membentuk dirhodium tetraacetate, Rh 2 (O 2 CCH 3) 4 dan pelbagai turunan yang mengandungi dua ligan tambahan — misalnya, air, piridin, atau tripenilfosfin — dalam keadaan pengoksidaan +2. Kompleks dalam keadaan pengoksidaan +1 terutama mengandungi karbon monoksida, olefin, dan fosfin sebagai ligan. Semua sebatian rhodium mudah dikurangkan atau diuraikan dengan pemanasan untuk menghasilkan serbuk atau logam span. Antara sebatian rhodium trichloride, RhCl 3 (di mana rhodium adalah di negeri ini 3), adalah salah satu yang paling penting. Ia menyediakan bahan permulaan bagi sebilangan besar sebatian rhodium lain dalam pelbagai keadaan pengoksidaan. Dalam emulsi berair, ia dapat menjadi pemangkin kepada sebilangan reaksi organik yang berguna.
Sifat Elemen
| nombor atom | 45 |
|---|---|
| berat atom | 102.905 |
| takat lebur | 1,966 ° C (3,571 ° F) |
| takat didih | 3,727 ° C (6,741 ° F) |
| graviti tertentu | 12.4 (20 ° C) |
| keadaan pengoksidaan | +1, +2, +3, +4, +5, +6 |
| konfigurasi elektron. | [Kr] 4d 8 5s 1 |