Konduktor, penebat, dan semikonduktor
Bahan dikelaskan sebagai konduktor, penebat, atau semikonduktor mengikut kekonduksian elektriknya. Pengelasannya dapat difahami dalam istilah atom. Elektron dalam atom hanya boleh mempunyai tenaga yang ditentukan dengan baik, dan, bergantung pada tenaganya, elektron dikatakan menempati tahap tenaga tertentu. Dalam atom khas dengan banyak elektron, tahap tenaga yang lebih rendah diisi, masing-masing dengan bilangan elektron yang dibenarkan oleh peraturan mekanikal kuantum yang dikenali sebagai prinsip pengecualian Pauli. Bergantung pada elemen, tahap tenaga tertinggi yang mempunyai elektron mungkin penuh atau tidak sepenuhnya. Sekiranya dua atom dari beberapa unsur dibawa cukup dekat sehingga saling berinteraksi, sistem dua atom mempunyai dua tahap jarak dekat untuk setiap tahap atom tunggal. Sekiranya 10 atom berinteraksi, sistem 10-atom akan mempunyai kelompok 10 tahap yang sesuai dengan setiap tahap satu atom individu. Dalam pepejal, bilangan atom dan oleh itu jumlah tahapnya sangat besar; sebahagian besar tahap tenaga yang lebih tinggi bertindih secara berterusan kecuali untuk tenaga tertentu di mana tidak ada tahap sama sekali. Kawasan tenaga dengan tahap disebut pita tenaga, dan wilayah yang tidak memiliki level disebut sebagai jurang pita.

Kuiz
Elektrik: Litar Pendek & Arus Langsung
Siapa yang menemui undang-undang elektrolisis?
Jalur tenaga tertinggi yang diduduki oleh elektron ialah pita valensi. Dalam konduktor, jalur valensi diisi sebahagian, dan kerana terdapat banyak tahap kosong, elektron bebas bergerak di bawah pengaruh medan elektrik; oleh itu, dalam logam pita valensi juga merupakan jalur konduksi. Dalam penebat, elektron mengisi jalur valensi sepenuhnya; dan jurang antara ia dan jalur seterusnya, yang merupakan jalur konduksi, adalah besar. Elektron tidak dapat bergerak di bawah pengaruh medan elektrik kecuali jika mereka diberi tenaga yang cukup untuk menyeberangi jurang tenaga yang besar ke jalur konduksi. Dalam semikonduktor, jurang ke jalur konduksi lebih kecil daripada pada penebat. Pada suhu bilik, jalur valensi hampir penuh. Beberapa elektron hilang dari pita valensi kerana mereka telah memperoleh tenaga haba yang cukup untuk menyeberangi jurang pita ke jalur konduksi; akibatnya, mereka boleh bergerak di bawah pengaruh medan elektrik luaran. “Lubang” yang tertinggal di jalur valensi adalah pembawa cas bergerak tetapi berkelakuan seperti pembawa cas positif.
Bagi banyak bahan, termasuk logam, ketahanan terhadap aliran muatan cenderung meningkat dengan suhu. Sebagai contoh, kenaikan 5 ° C (9 ° F) meningkatkan ketahanan kuprum sebanyak 2 peratus. Sebaliknya, ketahanan penebat dan terutamanya semikonduktor seperti silikon dan germanium menurun dengan cepat dengan suhu; peningkatan tenaga haba menyebabkan sebilangan elektron mengisi tahap di jalur konduksi di mana, dipengaruhi oleh medan elektrik luaran, mereka bebas bergerak. Perbezaan tenaga antara tahap valensi dan jalur konduksi mempunyai pengaruh yang kuat terhadap kekonduksian bahan-bahan ini, dengan jurang yang lebih kecil menghasilkan konduksi yang lebih tinggi pada suhu yang lebih rendah.
Nilai resistiviti elektrik yang disenaraikan dalam Jadual 2 menunjukkan variasi keupayaan bahan yang berbeza untuk mengalirkan elektrik yang sangat besar. Sebab utama untuk variasi yang besar adalah pelbagai ketersediaan dan mobiliti pembawa cas dalam bahan. Kawat tembaga dalam Rajah 12, misalnya, mempunyai banyak pembawa yang sangat mudah alih; setiap atom tembaga mempunyai lebih kurang satu elektron bebas, yang sangat mudah bergerak kerana jisimnya yang kecil. Elektrolit, seperti larutan air masin, tidak sebaik konduktor seperti tembaga. Ion natrium dan klorin dalam larutan memberikan pembawa muatan. Jisim besar setiap ion natrium dan klorin meningkat apabila ion-ion menarik yang lain berkumpul di sekelilingnya. Akibatnya, ion natrium dan klorin jauh lebih sukar dipindahkan daripada elektron bebas dalam tembaga. Air murni juga merupakan konduktor, walaupun airnya buruk kerana hanya sebilangan kecil molekul air yang dipisahkan menjadi ion. Gas oksigen, nitrogen, dan argon yang membentuk atmosfera agak konduktif kerana sebilangan pembawa cas terbentuk apabila gas-gas tersebut diionisasi oleh radiasi dari unsur-unsur radioaktif di Bumi dan juga dari sinar kosmik luar bumi (iaitu, inti atom berkelajuan tinggi dan elektron). Elektroforesis adalah aplikasi yang menarik berdasarkan pergerakan zarah yang digantung dalam larutan elektrolit. Zarah berlainan (protein, misalnya) bergerak di medan elektrik yang sama pada kelajuan yang berbeza; perbezaan kelajuan boleh digunakan untuk memisahkan isi gantungan.
Arus yang mengalir melalui wayar memanaskannya. Fenomena biasa ini berlaku pada gegelung pemanasan julat elektrik atau di filamen tungsten panas dari mentol lampu elektrik. Pemanasan ohmik ini adalah asas bagi sekering yang digunakan untuk melindungi litar elektrik dan mencegah kebakaran; jika arus melebihi nilai tertentu, sekering, yang diperbuat daripada aloi dengan takat lebur rendah, mencair dan mengganggu aliran arus. Kuasa P hilang dalam rintangan R di mana arus i mengalir diberikan oleh
di mana P berada dalam watt (satu watt sama dengan satu joule sesaat), saya berada dalam ampere, dan R berada dalam ohm. Menurut undang-undang Ohm, perbezaan potensial V antara dua hujung perintang diberikan oleh V = iR, dan daya P dapat dinyatakan sama seperti
Walau bagaimanapun, dalam bahan tertentu, pelesapan daya yang memanifestasikan dirinya sebagai haba tiba-tiba hilang sekiranya konduktor disejukkan ke suhu yang sangat rendah. Kehilangan semua rintangan adalah fenomena yang dikenali sebagai superkonduktiviti. Seperti yang telah disebutkan sebelumnya, elektron memperoleh beberapa kecepatan drift rata-rata v di bawah pengaruh medan elektrik dalam wayar. Biasanya elektron, dikenakan daya kerana medan elektrik, mempercepat dan secara progresif memperoleh kelajuan yang lebih besar. Kelajuan mereka, bagaimanapun, terhad dalam wayar kerana mereka kehilangan sebahagian tenaga yang mereka peroleh ke wayar dalam perlanggaran dengan elektron lain dan bertabrakan dengan atom dalam wayar. Tenaga yang hilang dipindahkan ke elektron lain, yang kemudian memancar, atau wayar menjadi teruja dengan getaran mekanikal kecil yang disebut sebagai fonon. Kedua-dua proses memanaskan bahan. Istilah fonon menekankan hubungan getaran ini dengan getaran mekanikal lain - iaitu bunyi. Dalam superkonduktor, kesan mekanik kuantum kompleks menghalang kehilangan tenaga kecil ke medium ini. Kesannya melibatkan interaksi antara elektron dan juga antara elektron dan bahan lain. Ia dapat dilihat dengan mempertimbangkan gandingan elektron berpasangan dengan momentum yang berlawanan; gerakan elektron berpasangan sedemikian rupa sehingga tidak ada tenaga yang diberikan hingga medium dalam perlanggaran elastik atau pengujaan fonon. Seseorang dapat membayangkan bahawa elektron yang akan "bertembung" dengan dan kehilangan tenaga ke media boleh berakhir sebaliknya bertabrakan dengan pasangannya sehingga mereka bertukar momentum tanpa memberikan apa-apa pada media.
Bahan superkonduktor yang banyak digunakan dalam pembinaan elektromagnet adalah aloi niobium dan titanium. Bahan ini mesti disejukkan hingga beberapa darjah di atas suhu sifar mutlak, −263.66 ° C (atau 9.5 K), untuk menunjukkan sifat superkonduktor. Penyejukan sedemikian memerlukan penggunaan helium cair, yang agak mahal. Pada akhir 1980-an, bahan yang menunjukkan sifat superkonduktor pada suhu yang jauh lebih tinggi ditemui. Suhu ini lebih tinggi daripada ogen196 ° C nitrogen cair, memungkinkan untuk menggunakan yang terakhir dan bukannya helium cair. Oleh kerana nitrogen cair banyak dan murah, bahan seperti itu dapat memberikan manfaat besar dalam berbagai aplikasi, mulai dari transmisi tenaga elektrik hingga pengkomputeran berkelajuan tinggi.
Daya elektromotif
Bateri automotif 12 volt dapat memberikan arus ke rangkaian seperti radio kereta untuk jangka masa yang panjang, di mana perbezaan potensi antara terminal bateri tetap hampir dengan 12 volt. Bateri mesti mempunyai kaedah untuk terus menambah kelebihan cas positif dan negatif yang terdapat di terminal masing-masing dan yang bertanggungjawab untuk perbezaan potensi 12 volt antara terminal. Caj mesti dibawa dari satu terminal ke terminal yang lain ke arah yang bertentangan dengan daya elektrik pada cas antara terminal. Mana-mana peranti yang melakukan pengangkutan cas ini merupakan sumber daya elektromotif. Bateri kereta, misalnya, menggunakan tindak balas kimia untuk menghasilkan daya elektromotif. Penjana Van de Graaff yang ditunjukkan dalam Rajah 13 adalah alat mekanikal yang menghasilkan daya elektromotif. Dicipta oleh ahli fizik Amerika Robert J. Van de Graaff pada tahun 1930-an, jenis pecutan zarah ini telah banyak digunakan untuk mengkaji zarah subatom. Kerana konsepnya lebih sederhana daripada sumber kimia daya elektromotif, penjana Van de Graaff akan dibincangkan terlebih dahulu.

Tali sawat penebat membawa muatan positif dari dasar mesin Van de Graaff ke bahagian dalam kubah pengalir besar. Cas dikeluarkan dari tali pinggang dengan jarak dekat elektrod logam tajam yang disebut titik penghilang cas. Cas kemudian bergerak pantas ke luar kubah pengalir. Kubah bermuatan positif menghasilkan medan elektrik, yang menjauh dari kubah dan memberikan tindakan penolakan pada cas positif tambahan yang diangkut pada tali pinggang ke arah kubah. Oleh itu, kerja dilakukan untuk memastikan tali sawat berpusing. Sekiranya arus dibiarkan mengalir dari kubah ke tanah dan jika arus yang sama disediakan oleh pengangkutan cas pada tali penebat, keseimbangan terjalin dan potensi kubah tetap pada nilai positif yang tetap. Dalam contoh ini, arus dari kubah ke tanah terdiri daripada aliran ion positif di dalam tiub pecutan, bergerak ke arah medan elektrik. Gerakan cas pada tali pinggang berada pada arah yang bertentangan dengan daya yang diberikan oleh medan elektrik kubah pada cas. Gerakan cas ini ke arah yang bertentangan dengan medan elektrik adalah ciri yang umum untuk semua sumber daya elektromotif.
Dalam keadaan daya elektromotif yang dihasilkan secara kimia, tindak balas kimia membebaskan tenaga. Sekiranya tindak balas ini berlaku dengan bahan kimia yang berdekatan antara satu sama lain (contohnya, jika ia bercampur), tenaga yang dibebaskan akan memanaskan campuran. Untuk menghasilkan sel voltan, tindak balas ini mesti berlaku di lokasi yang berasingan. Kawat tembaga dan wayar zink dicucuk ke dalam lemon membentuk sel voltik sederhana. Perbezaan potensi antara wayar tembaga dan zink dapat diukur dengan mudah dan didapati 1.1 volt; wayar tembaga bertindak sebagai terminal positif. "Bateri lemon" seperti itu adalah sel voltan yang agak lemah yang hanya dapat membekalkan sedikit tenaga elektrik. Jenis bateri 1.1 volt yang dibina dengan bahan yang pada dasarnya sama dapat menghasilkan lebih banyak elektrik. Dalam kes ini, wayar tembaga diletakkan dalam larutan kuprum sulfat dan kawat zink dalam larutan zink sulfat; kedua-dua penyelesaian disambungkan secara elektrik oleh jambatan garam kalium klorida. (Jambatan garam adalah konduktor dengan ion sebagai pembawa cas.) Dalam kedua-dua jenis bateri, tenaga berasal dari perbezaan tahap pengikatan antara elektron dalam tembaga dan yang ada dalam zink. Tenaga diperoleh apabila ion tembaga dari larutan kuprum sulfat didepositkan pada elektrod kuprum sebagai ion tembaga neutral, sehingga mengeluarkan elektron bebas dari wayar tembaga. Pada masa yang sama, atom zink dari wayar zink menjadi larutan sebagai ion zink bermuatan positif, meninggalkan wayar zink dengan elektron bebas berlebihan. Hasilnya adalah wayar tembaga bermuatan positif dan wayar zink bermuatan negatif. Kedua-dua reaksi dipisahkan secara fizikal, dengan jambatan garam melengkapkan litar dalaman.
Rajah 14 menggambarkan bateri asid plumbum 12 volt, menggunakan simbol standard untuk menggambarkan bateri dalam litar. Bateri terdiri daripada enam sel voltan, masing-masing dengan daya elektromotif kira-kira dua volt; sel disambungkan secara bersiri, sehingga enam voltan individu bertambah hingga sekitar 12 volt (Rajah 14A). Seperti yang ditunjukkan dalam Rajah 14B, setiap sel dua volt terdiri daripada sebilangan elektrod positif dan negatif yang disambungkan secara elektrik secara selari. Sambungan selari dibuat untuk menyediakan luas permukaan elektrod, di mana tindak balas kimia boleh berlaku. Kadar yang lebih tinggi di mana bahan elektrod dapat menjalani transformasi kimia membolehkan bateri memberikan arus yang lebih besar.
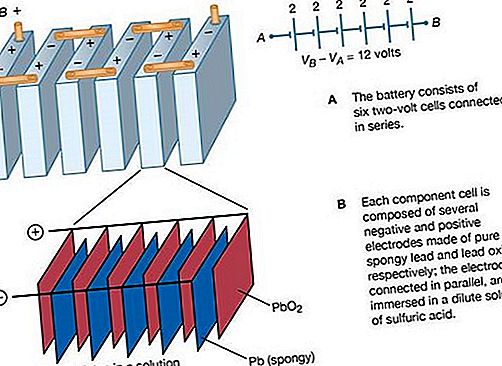
Dalam bateri asid plumbum, setiap sel voltan terdiri daripada elektrod negatif plumbum tulen (spb) dan elektrod positif oksida plumbum (PbO 2). Kedua-dua plumbum dan oksida plumbum berada dalam larutan asid sulfurik (H 2 SO 4) dan air (H 2 O). Pada elektrod positif, tindak balas kimia adalah PbO 2 + SO - / 4 - + 4H + + 2e - → PbSO 4 + 2H 2 O + (1,68 V). Pada terminal negatif, tindak balas adalah Pb + SO - / 4 - → PbSO 4 + 2e - + (0.36 V). Potensi sel ialah 1.68 + 0.36 = 2.04 volt. 1.68 dan 0.36 volt dalam persamaan di atas, masing-masing, adalah potensi pengurangan dan pengoksidaan; mereka berkaitan dengan pengikatan elektron dalam bahan kimia. Apabila bateri diisi semula, sama ada oleh penjana kereta atau oleh sumber kuasa luaran, kedua tindak balas kimia terbalik.
Litar arus terus
Litar arus terus (DC) yang paling sederhana terdiri daripada perintang yang disambungkan merentasi sumber daya elektromotif. Simbol bagi perintang ditunjukkan dalam Rajah 15; di sini nilai R, 60Ω, diberikan oleh nilai berangka yang berdekatan dengan simbol. Simbol bagi sumber daya elektromotif, E, ditunjukkan dengan nilai voltan yang berkaitan. Konvensyen memberikan terminal dengan garis panjang potensi yang lebih tinggi (iaitu, lebih positif) daripada terminal dengan garis pendek. Garis lurus yang menghubungkan pelbagai elemen dalam litar diasumsikan mempunyai rintangan yang dapat diabaikan, sehingga tidak ada perubahan potensi pada sambungan ini. Litar menunjukkan daya elektromotif 12 volt yang disambungkan ke perintang 60Ω. Huruf a, b, c, dan d pada rajah adalah titik rujukan.
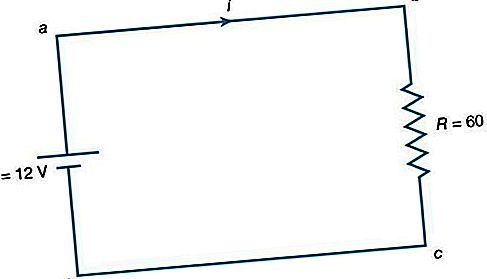
Fungsi sumber daya elektromotif adalah untuk mengekalkan titik a pada potensi 12 volt lebih positif daripada titik d. Oleh itu, perbezaan potensi V a - V d ialah 12 volt. Perbezaan potensi merintang adalah V b - V c. Dari undang-undang Ohm, arus yang mengalir melalui perintang adalah
Oleh kerana titik a dan b dihubungkan oleh konduktor rintangan yang dapat diabaikan, mereka berpotensi sama. Atas sebab yang sama, c dan d berpotensi sama. Oleh itu, V b - V c = V a - V d = 12 volt. Arus dalam litar diberikan oleh persamaan (24). Oleh itu, i = 12/60 = 0.2 ampere. Daya yang hilang dalam perintang kerana haba dikira dengan mudah menggunakan persamaan (22):
Dari mana datangnya tenaga yang hilang ketika haba dalam perintang? Ini disediakan oleh sumber daya elektromotif (contohnya, bateri asid plumbum). Dalam sumber seperti itu, untuk setiap jumlah caj dQ dipindahkan dari potensi yang lebih rendah pada d ke potensi yang lebih tinggi pada a, sejumlah pekerjaan dilakukan sama dengan dW = dQ (V a - V d). Sekiranya kerja ini dilakukan dalam selang waktu dt, kuasa yang dihantar oleh bateri diperoleh dengan membahagi dW dengan dt. Oleh itu, kuasa yang dihantar oleh bateri (dalam watt) adalah
Menggunakan nilai i = 0.2 ampere dan V a - V d = 12 volt menjadikan dW / dt = 2.4 watt. Seperti yang dijangkakan, kuasa yang dihantar oleh bateri sama dengan daya yang hilang ketika panas di perintang.












![Filem The Man with the Golden Arm oleh Preminger [1955] Filem The Man with the Golden Arm oleh Preminger [1955]](https://images.thetopknowledge.com/img/entertainment-pop-culture/2/man-with-golden-arm-film-preminger-1955.jpg)
